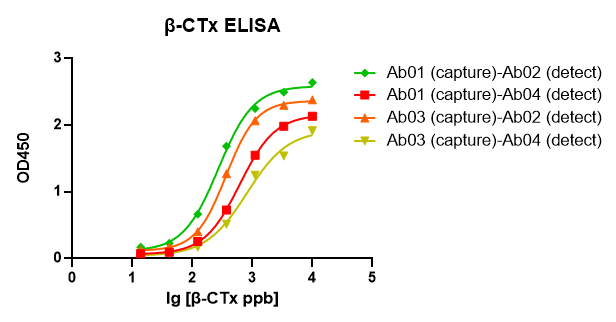
Исследования показали, что активированные остеокласты создают ямки резорбции с низким pH для растворения неорганической матрицы, а лизосомные ферменты, такие как TRAP и катепсин K, эффективно расщепляют обнаженный коллаген первого типа, высвобождая специфические продукты разложения, такие как карбокси-концевые сшитые телопептиды коллагена I типа (CTX-1). Биомаркер β-CTx предоставляет значительную информацию о метаболизме костей (перестройке костей) и полезен для прогнозирования риска переломов и мониторинга эффективности лечения. Недавно наш исследовательский отдел продемонстрировал, что наши пары GMP-h-β-CTx-Ab обладают широким линейным диапазоном и хорошей чувствительностью к GMP-h-β-CTx-Ag01. Ниже приведены результаты проверки пар GMP-h-β-CTx-Ab01/02/03/04 от GeneMedi (моноклональные антитела мыши против человеческого β-CTx) на выявление GMP-h-β-CTx-Ag01 (рекомбинантный человеческий β-CTx белок) в ELISA. Мы настоятельно рекомендуем пары Ab01-Ab02 и Ag.
Полная информация о примере исследования доступна по ссылке: https://www.genemedi.net/i/data-case-study-25-OH-VD
Общая способность идентификации 25-OH-VD
Сэндвич-антитела GeneMedi против 25-OH-VD (GMP-SMT-25-OH-VD3/2-Ab01 и GMP-SMT-25-OH-VD3/2-Ab02) были проверены на платформе прямой хемилюминесценции. Благодаря хорошей перекрестной реактивности с 25-OH-VD2 и 25-OH-VD3, можно успешно определить общее количество 25-OH-VD в образце.
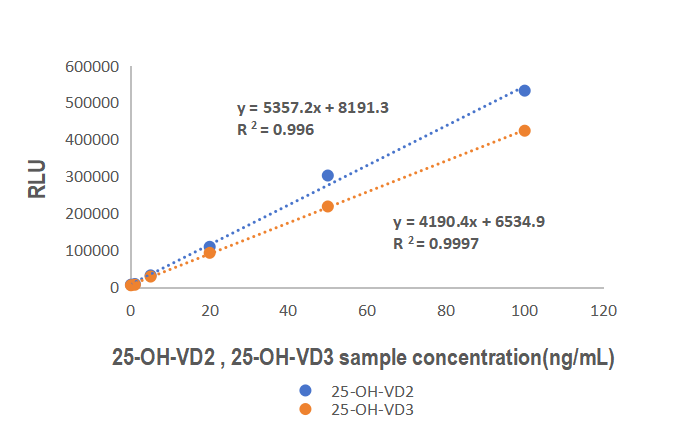
Рисунок 1. Общая способность распознавания 25-OH-VD; Как видно на рисунке выше, 25-OH-VD2 и 25-OH-VD3 демонстрируют хорошую перекрестную реактивность.
Коэффициент совпадения образцов
Сэндвич-антитела против VD от GeneMedi были проверены на платформе прямой хемилюминесценции с использованием золотого стандарта индустрии LC-MS/MS в качестве контроля, чтобы повысить точность иммуноанализа 25-OH-VD. По сравнению с результатами масс-спектрометрии, эти антитела показали отличное согласование, с R2 до 0.9718 и подтвержденным клиентом R2 0.963. Сэндвич-метод значительно улучшил точность иммуноанализа.
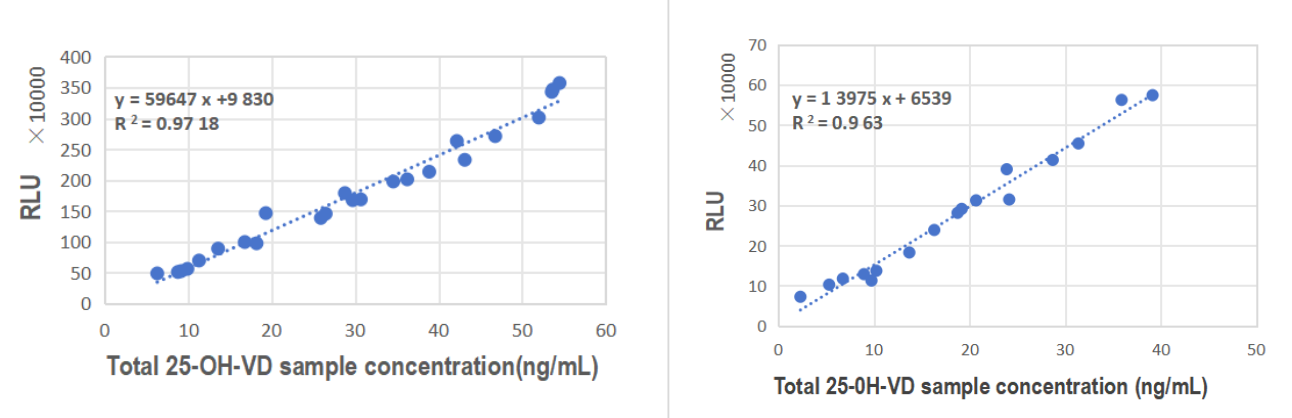
Рисунок 2. Самостоятельный клинический сравнительный анализ и клинический сравнительный анализ, подтвержденный клиентом; Эти антитела показали отличное согласование по сравнению с результатами масс-спектрометрии, с R2 до 0.9718 и подтвержденным клиентом R2 0.963. Сэндвич-метод значительно улучшает точность иммуноанализа.
Кривая стандартного образца
Диапазон обнаружения концентраций для сэндвич-антител GeneMedi против 25-OH-VD (GMP-SMT-25-OH-VD3/2-Ab01 и GMP-SMT-25-OH-VD3/2-Ab02) составляет от 0.1 до 80нг/мл.
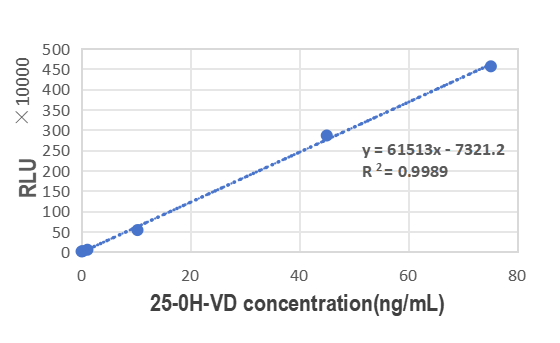
Рисунок 4. Кривая стандартного образца; Как видно на рисунке выше, диапазон обнаружения концентраций для сэндвич-антител GeneMedi против 25-OH-VD составляет от 0.1 до 80нг/мл.
Коэффициент совпадения образцов
Обнаружение с использованием сэндвич-антител против 25-OH-VD (GMP-SMT-25-OH-VD3/2-Ab01 и GMP-SMT-25-OH-VD3/2-Ab02), проверенных на платформе ферментативной хемилюминесценции, продемонстрировало сильное согласование с использованием масс-спектрометрии (LC-MS/MS) с R2 0.9741.
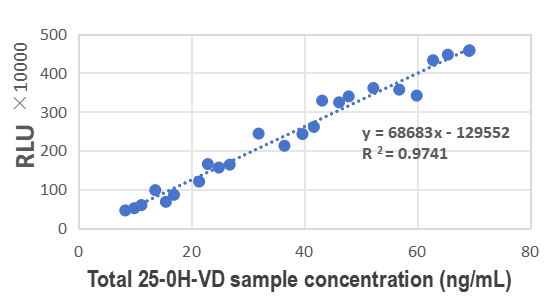
Рисунок 5. Клинический сравнительный анализ; Как видно на рисунке выше, обнаружение с использованием сэндвич-антител против 25-OH-VD, проверенных на платформе ферментативной хемилюминесценции, показало сильное согласование с использованием масс-спектрометрии (LC-MS/MS) с R2 0.9741.
Разработаны новые биологические маркеры, и исследования показывают, что они могут быть ценными исследовательскими инструментами для изучения механизмов метаболизма костей и оценки активности остеоцитов. Некоторые из них могут быть ценными для управления пациентами с остеопорозом и другими заболеваниями костей. Чтобы лучше прогнозировать риск переломов и мониторить эффективность лечения остеопороза и других заболеваний костей, GDU предлагает диагностические антитела и антигены для таких биомаркеров, как CTX-1, P1NP, N-MID OC, PTH и 25-OH-VD. Эти биомаркеры можно использовать на панели метаболизма костей.
| Cat No. | Biomarker | Physiological process | Clinical value |
| GMP-h-β-CTx | β-isomerized C-terminal telopeptides (β-CTx), Beta-CrossLaps (beta-CTx) | Bone resorption | Evaluate bone resorption rate |
| GMP-h-PINP | procollagen type I N-terminal propeptide (PINP), amino-terminal propeptide of type 1 procollagen (P1NP) | Bone formation | Evaluate bone formation rate |
| GMP-h-N-MID-OC | N-terminal midfragment of Osteocalcin (N-MID OC) | Bone formation | Evaluate bone formation rate |
| GMP-h-PTH | parathyroid hormone (PTH) | Calcium cycle | Evaluate hypercalcemia/ hypocalcemia/ hyperparathyroidism |
| GMP-SMT-25-OH-VD3/2 | 25 hydroxyvitamin D (25-OH-(VD3+VD2)) | Calcium cycle | Evaluate vitamin D sufficiency |
| GMP-SMT-25-OH-VD-3 | 25-hydroxy (OH) Vitamin D3 (25-OH-VD-3) | Calcium cycle | Evaluate vitamin D sufficiency |
Кости не являются инертными структурами в организме человека; они продолжают изменяться на протяжении всей жизни. Обмен веществ в костях характеризуется тесным сотрудничеством костных клеток, включая остеобласты, остеокласты и остеоциты, для поддержания количества костной ткани и целостности костной структуры. Этот процесс изменения костей также известен как ремоделирование костей, которое защищает структурную целостность скелетной системы и метаболически способствует балансу кальция и фосфора в организме. Ремоделирование включает резорбцию старых или поврежденных костей, за которой следует отложение нового костного материала. Этот процесс в основном регулируется разрушением костей остеокластами и образованием костей остеобластами. Кроме того, остеоциты также играют роль в этом процессе.
Цикл ремоделирования костей длится 150-200 дней и в основном осуществляется сигналами остеобластов, которые способствуют дифференцировке и созреванию предшественников остеокластов. Активированные остеокласты создают резорбционные ямы с низким уровнем pH для растворения неорганической матрицы, а лизосомальные ферменты, такие как TRAP и катепсин K, эффективно переваривают обнаженный коллаген 1 типа, высвобождая специфические продукты распада, такие как телопептиды карбоксильного конца связанного коллагена 1 типа (CTX-1). Остеобласты притягиваются к этой эрозированной поверхности и начинают образовывать новую остеоидную ткань. Коллаген 1 типа, обильный в остеобластах, секретируется в виде предшественника молекулы проколлагена в внеклеточное пространство, где он расщепляется на аминном и карбоксильном концах, высвобождая пропептиды в кровь. Пропептид N-концевого проколлагена типа I (P1NP) и остеокальцин (OC) являются наиболее чувствительными маркерами скорости образования костей. Анализ целого остеокальцина (iOC) установлен как стандартный анализ для оценки функции остеобластов. Исследование клинической полезности нового иммуннорадиометрического анализа для остеокальцина (OC), который определяет стабильный N-концевой средний фрагмент OC (анализ N-MID OC), показывает, что иммунореактивность N-MID OC гораздо стабильнее, чем иммунореактивность iOC, и что анализ N-MID OC может быть менее восприимчив к фрагментам OC, которые накапливаются в уремической сыворотке. Поэтому он может оказаться более надежным, чем анализ iOC, для оценки обмена веществ в костях и, следовательно, для отражения потери костей. Сначала гидроксиапатитовые кристаллы откладываются в остеоиде, затем медленный процесс минерализации продолжается несколько месяцев, за которым следует период покоя. RANKL, необходимый остеокластогенезирующий цитокин, экспрессируется на поверхности остеобластов, связывается с его клеточным рецептором RANK на предшественниках остеокластов и способствует их дифференцировке и активации. OPG, ложный рецептор для RANKL, секретируется остеобластами и другими клетками, происходящими из стромы, и уменьшает резорбцию костей, связываясь с RANK и предотвращая активность остеокластов.
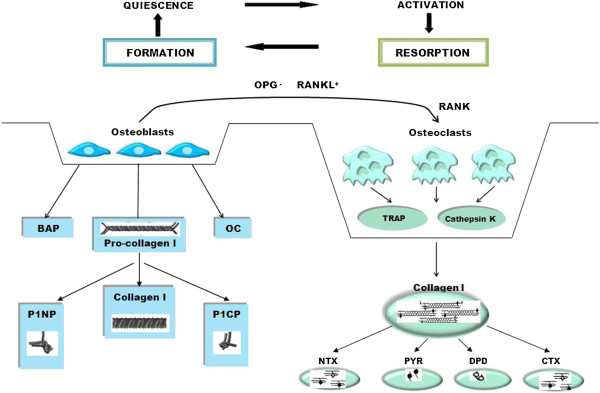
Рисунок 2. Цикл обмена веществ в костях (ремоделирование костей).
Кальций как питательное вещество наиболее часто ассоциируется с формированием и обменом веществ в костях. Костная ткань служит резервуаром и источником кальция для этих критических метаболических потребностей через процесс ремоделирования костей. Обмен кальция в основном регулируется эндокринной системой паратиреоидного гормона (PTH)-витамина D, которая характеризуется серией гомеостатических обратных связей. Быстрое высвобождение минералов из костей необходимо для поддержания адекватного уровня ионизированного кальция в сыворотке. При дефиците витамина D обмен веществ в костях значительно нарушается из-за уменьшения активного всасывания кальция. Это приводит к увеличению секреции PTH, поскольку кальциевый сенсорный рецептор в паращитовидной железе обнаруживает изменения в циркулирующем ионном кальции. Увеличение уровня PTH вызывает активность фермента (1α-гидроксилазы) в почках, который превращает витамин D в его активную гормональную форму, кальцитриол. В свою очередь, кальцитриол стимулирует повышенное всасывание кальция из кишечника. Неудивительно, что взаимодействие между динамикой кальция и витамина D часто усложняет интерпретацию данных относительно потребностей в кальции, состояний дефицита и избытка потребления.
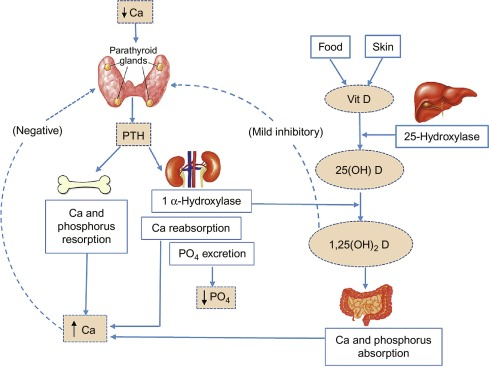
Рисунок 3. Кальциевый цикл.
При метаболических заболеваниях костей, таких как остеопороз, обмен веществ в костях нарушается, что приводит к потере костной массы, сопровождающейся изменениями в микроархитектуре, что приводит к хрупкости костей и, в конечном итоге, к переломам.
Остеопороз - это системное скелетное заболевание, характеризующееся низкой костной массой, ухудшением микроархитектуры костной ткани, что приводит к хрупкости костей и, следовательно, к увеличению риска переломов. Это наиболее частая причина переломов у пожилых людей. Кости, которые обычно ломаются, включают позвонки в позвоночнике, кости предплечья и тазобедренный сустав. До перелома обычно нет симптомов. Кости могут ослабнуть до такой степени, что перелом может произойти при незначительном стрессе или спонтанно. После заживления перелома у человека могут возникнуть хронические боли и снижение способности выполнять обычные действия. Мониторинг пациентов, получающих лечение от остеопороза, должен включать регулярные контакты с медицинским специалистом, чтобы убедиться, что: (1) лекарства принимаются регулярно и правильно, (2) потребление кальция и витамина D является достаточным, (3) у пациента нет побочных эффектов или страха перед побочными эффектами, которые необходимо учитывать, и (4) нет сопутствующих заболеваний или других лекарств, которые могут изменить ожидаемый эффект лечения.
Разработка сывороточных и мочевых анализов для биохимических маркеров, отражающих либо ферментативную активность остеобластов и остеокластов, либо продукты распада костной ткани, была очень полезна для изучения сложных путей обмена веществ в костях и их изменений при костных заболеваниях. Такие биомаркеры, как CTX-1, P1NP, N-MID OC, PTH и 25-OH-VD, предоставляют важную информацию о метаболизме костей (ремоделировании костей) и кальциевом цикле и полезны для прогнозирования риска переломов и мониторинга эффективности лечения.

